全球有數百萬人已接種預防新冠肺炎的mRNA疫苗,此篇文章可快速了解疫苗在人體的臨床運作模式。
RNA(mRNA)疫苗技術已推出一段時間,但直到最近才接到mRNA疫苗可被授權使用;也因此每位患者和各醫療服務單位對於疫苗的製作和運作模式仍存在很多疑問。
一開始儘管我們會較熟悉DNA去氧核糖核酸 ,但對於在高中生物課學過的mRNA信使核糖核酸可能不會留下甚麼印象;DNA通常被視為細胞的設計藍圖,而蛋白質則是組成這個結構的物質;藉這個常用的比喻,mRNA就如同藍圖下達的指令來製造該結構所有的成分,而DNA的每個基因都會被轉錄成細胞核中的mRNA訊息,然後這個mRNA會跑到細胞質再由核醣體轉譯成蛋白質後就自然捨棄分解。
DNA → mRNA → Protein
去氧核糖核酸DNA轉錄至信使核糖核酸mRNA再轉譯至蛋白質Protein
我們多年來的研究都在深入瞭解如何讓mRNA能更穩定及如何將它包入脂質奈米微粒囊來送進細胞裡,雖然這個領域的研究仍在不斷演進,但當新冠肺炎COVID-19疫情爆發時,這方面的知識就已具備。因此為了要製造對付冠狀病毒疾病COVID-19的mRNA疫苗,最需要的就是病原體上目標抗原的基因序列;用SARS-CoV-2來看就是棘蛋白基因,自2020年1月SARS-CoV-2的基因序列被定序後不久,具有mRNA技術專長的製藥公司,包括BioNTech與莫德納在內就開始製造對付冠狀病毒疾病的mRNA疫苗。
在這兩種mRNA疫苗中,唯一具有活性成分是mRNA本身,其較重要的是mRNA無法改變細胞中的DNA,主要是疫苗永遠不會進入DNA所在的細胞核;這些mRNA疫苗也含有脂質能保護mRNA並協助成分進入細胞、鹽、糖及具有穩定作用的緩衝溶液,這些疫苗之間的特定脂質和安定劑有所不同,但這兩種mRNA疫苗都已證實是安全的且整體過敏性反應為每百萬劑裡少於5件個案。
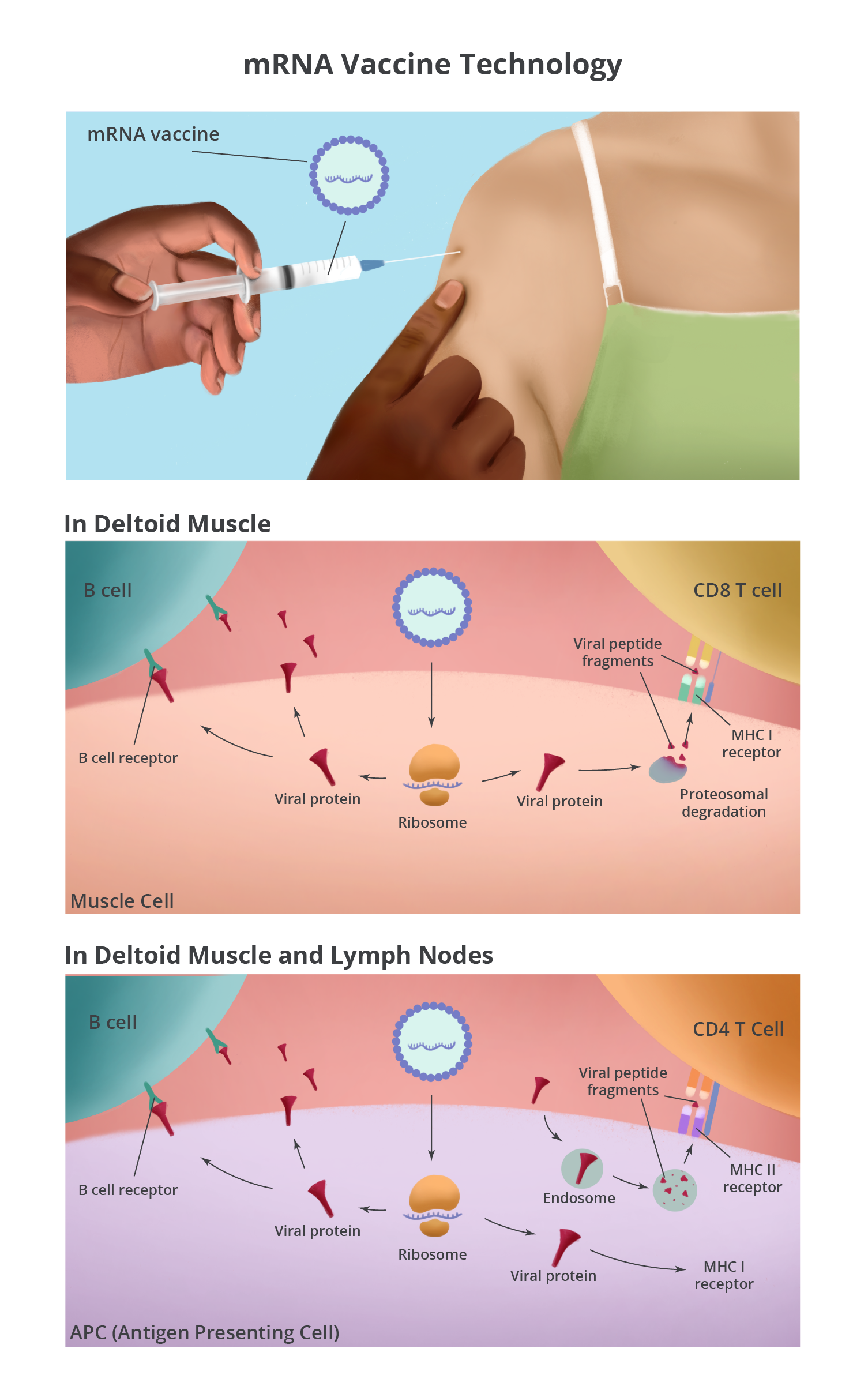
這兩種mRNA疫苗都是用肌肉注射到手臂的三頭肌位置,由於脂質奈米微粒具有疏水性,因此疫苗能附著在細胞膜上,一旦這些脂質與肌肉細胞結合,mRNA就會被釋放到細胞的細胞質裡;在細胞質內的疫苗mRNA就會發揮像細胞mRNA一樣的作用,也就是被核醣體轉譯成蛋白質 – 在此狀況則是SARS-CoV-2棘蛋白在注射位置周圍的肌肉細胞會產生大量的棘蛋白,而這些棘蛋白就會被組織中的免疫細胞察覺。
注射的位置會形成一處刺穿的傷口,然後一劑量的疫苗被注入組織當中在兩者加在一起,就會造成細胞壓力並警告免疫系統可能有狀況發生,此外mRNA本身也被當作激起發炎反應而引起一連串的免疫反應;這種發炎及壓力反應會將免疫細胞帶到該處肌肉,於是才會造成手臂注射位置出現疼痛、腫大與泛紅。
抗原呈現細胞(APCs)就是被帶到該處位置的一種免疫細胞,mRNA疫苗能夠進入APCs再製造棘蛋白(就如同它在肌肉細胞中的作用一樣)並刺激B細胞與CD8 T細胞;此APCs細胞所扮演的另一種關鍵角色是藉著拾取注射位置的細胞外蛋白質、死細胞與碎片來啟動人體的免疫反應,此方式能分解包括棘蛋白在內的各種蛋白質且向CD4 T細胞呈現勝肽碎片;另外APCs細胞也不是處於靜止狀態,其將注射位置的抗原帶至該處的引流淋巴結,即能更容易遇到B細胞、CD4 T細胞及CD8 T細胞,而這些細胞的受體都能辨識棘蛋白。
一旦特定抗原的淋巴細胞被啟動就會開始增生並從初始細胞分化成作用細胞,作用型B細胞主要功能是製造抗體,抗體有不同的種類並各自執行不同任務;接種疫苗後產生的抗體的一項重要功能就是中和作用(纏住病毒、阻止感染細胞),而作用型CD4 T細胞具有相當廣泛的功能,包括協助B細胞製造針對最優先目標抗體來抑制免疫反應,作用型CD8 T細胞則通常被叫做細胞毒性T細胞,這是因為此細胞會對身體進行詳細檢查再消滅被感染的細胞;有時候這整個免疫活動會引起系統性症狀,像是發燒、倦怠感和肌肉疼痛,這都是在接種後出現的正常反應,也可稱為反應原性(reactogenicity)且通常在接種第二劑mRNA疫苗後較為發生。
接種疫苗產生最深遠的影響是某些作用細胞會繼續存在且會保留對於SARS-CoV-2棘蛋白的記憶(這些細胞叫做記憶型B細胞與記憶型T細胞);若已接種的人感染SARS-CoV-2,那麼在其體內循環的抗體會先纏住這種病毒,然後記憶型B細胞與記憶型T細胞會接著啟動快速、強烈的免疫反應來清除這種病毒;我們用mRNA疫苗來說,這種免疫反應可在95%的人身上預防感染症狀並在100%的人身上防止冠狀病毒疾病造成的重症與死亡。
不過雖然mRNA疫苗可說是一種嶄新的臨床醫學技術,但就像以往其他疫苗一樣也要需要進行受臨床試驗評估;基於很多種原因有可能在一年內就會加快新冠肺炎COVID-19疫苗的核准與配送;首先多年以來針對常見感冒冠狀病毒的研究及對SARS與MERS病毒的研究都有助於認識棘蛋白可能是疫苗的關鍵標的;其次是由於這方面的需求非常迫切,也因此即使要冒極大的財務風險,許多藥廠還是會在進行臨床前置研究的同時就已展開臨床試驗;最後一項重點則是新冠肺炎蔓延得很嚴重,在我們斷定疫苗效力所花的時間就不會像以往其他在預防較不常見感染的疫苗來得那麼長。
目前全球已有數億人完成疫苗接踵,似乎新冠肺炎COVID-19的mRNA疫苗是較安全有效的選擇且未來勢必會成為終結此疫情的重要利器。